Стереохимия sp3-гибридного углерода – два центра
Молекулы с двумя стереоцентрами рядом также изображают проекциями Фишера и естественными проекциями. Хотя можно было бы просто использовать уже известные приемы для одного стереоцентра, здесь есть свои особенности и лучше сразу их освоить.
Проекции Фишера для двух соседних стереоцентров довольно удобны. Сразу привыкнем к тому, что их изображают всегда вертикально и никогда горизонтально. Проекция Фишера всегда соответствует заслоненной конформации. Вертикально расположенные связи уходят назад (средняя находится в плоскости), горизонтальные идут вперед. Такую промежуточную проекцию нужно дальше взять за среднюю связь и опрокинуть – получится естественная проекция для заслоненной конформации. Так как такая конформация неустойчива, прокрутим структуру вокруг средней связи на 180 градусов. Вот это и будет естественная проекция, которую и нужно рисовать в первую очередь.
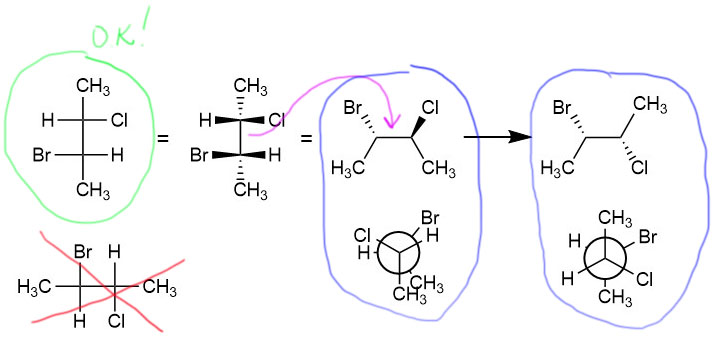
Теперь немного наведем порядок. Возьмем еще раз исходного Фишера и полученную из него проекцию. Совсем красиво, если мы ее чуток подразвернем прямо в плоскости бумаги, так чтобы то, что в Фишере было вертикалью стало бы вытянутой цепью. Все остальное уже пристроено. Именно так это и рисуют в современной литературе, и неплохо сразу привыкать к современной структурной графике. Почему это хорошо? Прежде всего, потому что удобно. Более того, если запомнить, как это делается для двух стереоцентров, вы без труда нарисуете и цепь с любым количеством стереоцентров (например, углевод какой-нибудь), не затратив более одной лишней секунды на центр. Если запомнить такой шаблон, то преобразование Фишера в естественную проекцию станет совершенным пустяком.
Итак,
- рисуем вертикаль из проекции Фишера змейкой с поднятой головой. Договариваемся смотреть на Фишера сверху (невероятная наглость, если учесть что Э.Фишер, возможно, самый великий химик-органик всех времен и народов), поэтому верхний атом будет справа.
Запоминаем три вещи:
- первый сверху центр рисуем так, что то, что в Фишере было справа, пойдет зеброй назад (соответственно, левая группа пойдет клином вперед);
- водороды на стереоцентрах не рисуем;
- второй центр рисуем относительно первого, имея в виду, что то, что в Фишере было в разные стороны здесь пойдет в одну (направо-налево даст две зебры, и т.п.). Если на каком-то центре оба заместителя не водороды, изображаем соотвественно.
Все. Шаблон и примеры:
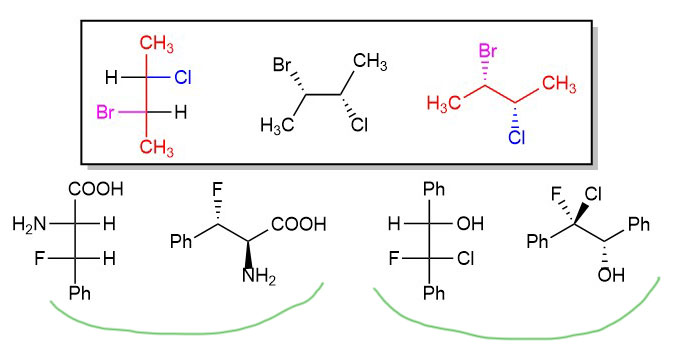
Изобразим для тренировки что-нибудь посолиднее, например, D-глюкозу аж с четырьмя стереоцентрами. Фишера для глюкозы можно найти везде, а вот естественную проекцию быстро рисовать умеют не все. И напрасно – чтобы читать современную литературу, лучше привыкать к более информативной и менее формальной естественной структурной графике. Итак, вертикаль Фишера рисуем змейкой с поднятой головой, обозначаем группы на концах цепи, находим первый сверху стереоцентр и обозначаем его так же, как уже научились для структур с двумя центрами; каждый следующий стереоцентр обозначаем относительно предыдущего (второй относительно первого, третий относительно второго, четвертый относительно третьего) тоже таким же образом. Задача с многими центрами поэтому сводится к задаче с двумя центрами. Получается довольно симпатично и гораздо компактнее Фишера, которого, будь там хоть сто центров, принято рисовать вертикально. К тому же на такой структуре очень удобно размечать R/S-конфигурации отдельных центров: для каждого просто нарисуйте стрелку убывания старшинства (да, слои снимать придется иногда до упора и закипания мозга). Конфигурация будет соответствовать направлению, там где OH спереди (клином), и быть обратной, там где OH сзади (зеброй). Как конкретно легко и быстро определить абсолютный конфигурации и разметить R/S-обозначения можно посмотреть на странице Ответы.
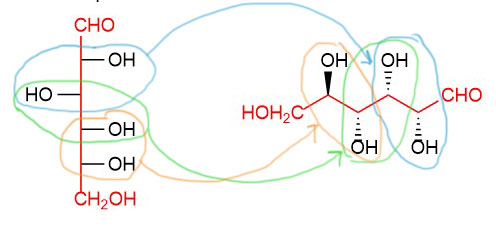
И еще одно пояснение. В естественной проекции клинышком и зеброй показывают определенную и известную конфигурацию стереоцентра. В некоторых случаях конфигурация неизвестна или сознательно скрыта. Для изображения таких неопределенных конфигураций используют волнистую линию (которую нужно умудриться не спутать с зеброй). Такое обозначение никогда не применяют в Фишере. Неопределенными могут быть как все, так и некоторые стереоцентры.
Что такое эритро и трео? Какая это номенклатура?
Никакая. Эритро и трео – это традиционные обозначения относительной стереохимической конфигурации двух соседних стереоцентров, укоренившиеся в органической химии с начала 20 века Похожих обозначений в стереохимии десятки, а возможно и сотни, но эти две приставки используются чаще других, потому что относятся к очень важному и распространенному случаю, когда в молекуле есть два стереоцентра на соседних атомах углерода. Строго говоря, эти обозначения описаны в стереохимической части номенклаьуры ИЮПАК, то есть являются признанными и в некотором смысле систематическими, но ИЮПАК никак не формализовала эти уже давно сложившееся обозначения, поэтому это просто очередной пример того, как номенклатура ИЮПАК соглашается на некоторые названия, сложившиеся в реальной химии по аналогии с тривиальными названиями. Например, ИЮПАК соглашается оставить название “уксусная кислота” и не обязательно всегда заменять его на этановую кислоту, но значит ли это, что название “уксусная кислота” стало систематическим? Нет, конечно, это просто означает, что создатели номенклатуры, на мой взгляд, мудро не стали ломать привычные химикам названия. То же и с эритро- и трео. Удобно и наглядно, давайте оставим.
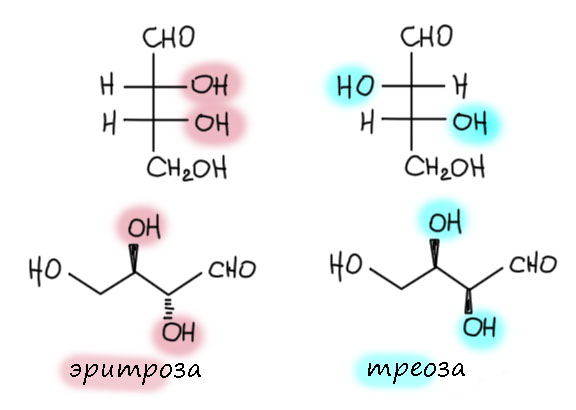
Эти обозначения всегда даются по аналогии, и сами слова происходят от каких-то знаменитых молекул, с которыми сравнивают другие молекулы. В данном случае в качестве молекул сравнения используют углеводы с 4 атомами углерода – эритрозу и треозу. Эритро– поэтому буквально означает – как в эритрозе, а трео– – как в треозе. В этих углеводах по два стереоцентра на соседних (втором и третьем) атомах углерода, на которых сидят гидрокси-группы. Вот они (для каждой показан только один энантиомер, так называемая D-форма, что это такое разберемся позже, пока это соверешенно не важно, потому что эритро и трео обозначают диастереомеры, а не энантиомеры) показаны в виде Фишера и в естественной проекции, как договорились, змейкой с головой вверх. Видим, что гидрокси-группы в эритрозе на Фишере изображаются в одну сторону (обе вправо или обе влево, в зависимости от энантиомера), а на естественной проекции с вытянутой цепью – в разные сторона (клин-зебра или зебра-клин). В треозе ровно все наоборот – на Фишере в разные стороны, а на проекции с вытянутой цепью в плоскости – в одну сторону. Один раз запомнил – и пользуйся!
По аналогии любые молекулы с двумя соседними стереоцентрами удобно обозначать этими приставками, если два заместителя на Фишере в одну сторону, то это эритро (в натуральной вытянутой змейке – в разные стороны). В трео – все наоборот. Это удобно и однозначно, если на каждом из центров один из атомов – водород. Вот примеры. Комментарии излишни, так как все очевидно. Приставку приделывают к названию спереди. Заместители могут быть одинаковыми или разными, и даже дейтерий вполне сойдет.
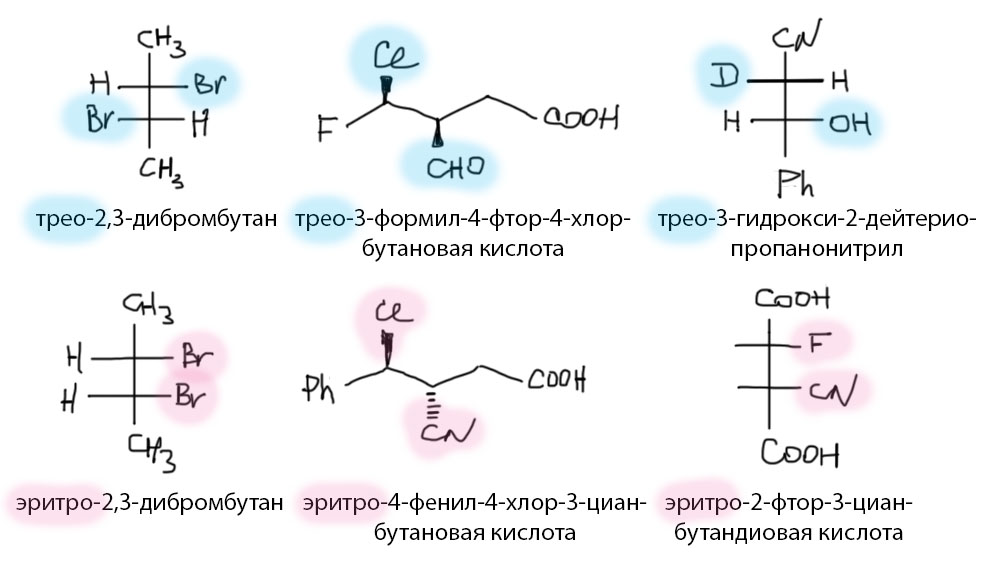
Сложности возникают тогда, когда на стереоцентрах нет водорода, и все группы разные. Сложность связана с тем, что в эритро/трео обозначениях не используется определение старшинства заместителей. Почему? Да просто не сложилось. Эритро/трео обозначения возникли очень давно, когда абсолютные конфигурации еще известны не были, и использовались в рядах близкородственных соединений, где интуитивно понятно, о чем идет речь. В номенклатуру эти обозначения не включались – в этом нет большого смысла, так как R/S обозначения дают полную информацию о стереохимической конфигурации, и как-то их еще дублировать смысла нет. Но R/S обозначения неудобны, так как их нужно для каждого центра вычислять, что для сложных молекул является процессом весьма нетривиальным. А эритро и трео видно сразу. Вообще-то хорошо бы и их как-то формализовать, и это можно было бы элементарно сделать, добавив какие-нибудь правила старшинства. Но – это сразу убило бы наглядность. Вот так и живем.
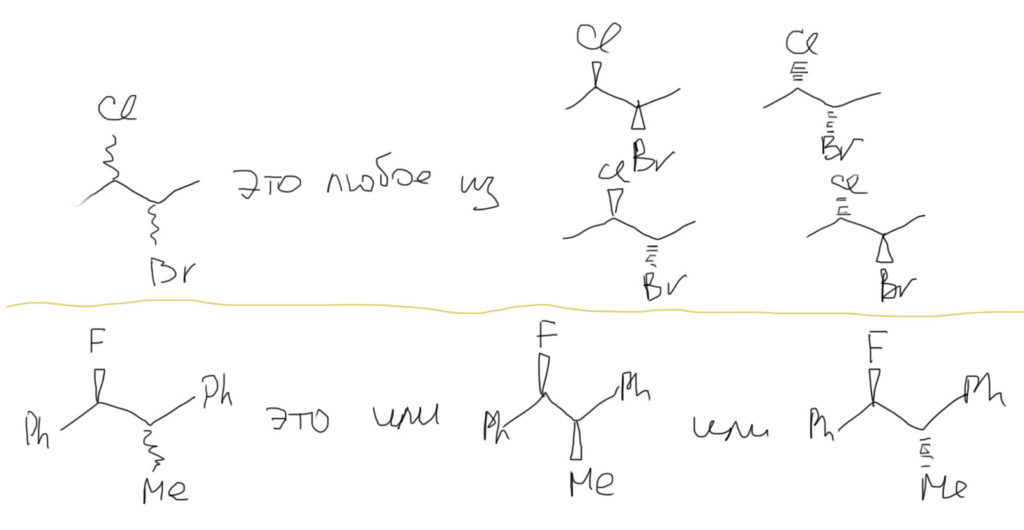
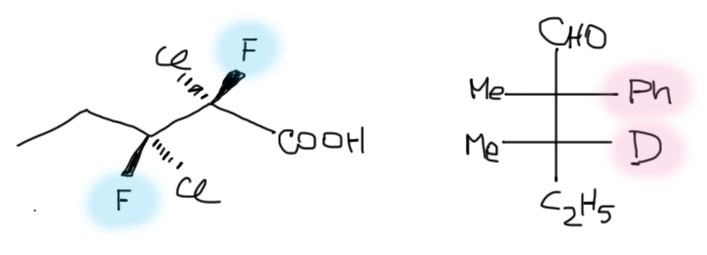
Отсюда вывод – эритро-трео обозначения нельзя использовать в названиях соединений с более сложными стереоцентрами, на которых нет одного водорода. Но очень даже можно и даже весьма популярно использовать эти приставки не в названиях, а в обозначении конфигурации словами. Например, некто рассуждает о 2,3-дифтор-2,3-дихлорпентановой кислоте с трео-расположением атомов фтора, или об эритро-конфигурации фенила и дейтерия в 3-дейтерио-2,3-диметил-2-фенилпентанале. Нарисуем эти структуры для тренировки разными проекциями (опять – обозначен только один из энантиомеров).
Еще раз повторим, что эритро и трео обозначения в любом варианте относятся только к диастереомерам. Энантиомеры так обозначить нельзя, и необходимо использовать R/S-номенклатуру. Каждый из эритро и трео диастереомеров представлен энантиомерной парой (которая иногда может быть вырождена в мезо-форму, если молекула оказывается нехиральной: только эритро-диастереомеры могут быть нехиральной мезо-формой, трео-диастереомеры всегда хиральны).
