Методы и задачи в химии соединений азота
Главная проблема этого раздела – чрезвычайная пестрота. Сюда собраны все соединения азота: нитросоединения, амины, диазосоединения, ароматические и алифатические, и то, если брать только основные группы соединений. И еще понемногу нитрозо-соединений, гидразинов, гидроксиламинов и т.п. Амиды у нас в карбоновых кислотах.
Основной класс веществ в этом разделе – амины, все остальное носит в существенной степени вспомогательный характер.
Новые C-C связи
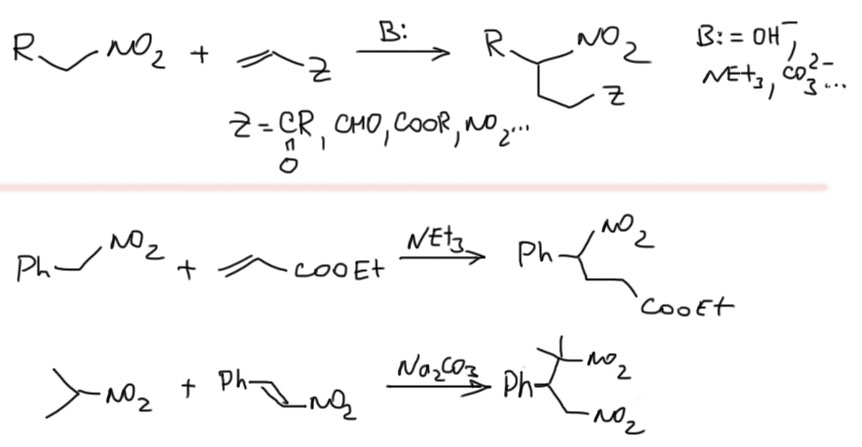
Второе важное обстоятельство – одна нитро-группа более мощный акцептор, чем два карбонила. Поэтому мононитросоединения обладают большей CH-кислотностью, чем малоновый или ацетоуксусный эфиры. Для депротонирования нитросоединений достаточно таких оснований как амины или карбонат, и не нужны не только LDA, но и этилат. Так как нитро-соединения еще и не дают самоконденсации, то реакции с ними проводят наиболее простым способом, добавляя основание к смеси нитросоединения и электрофила.
Конденсация с альдегидами и кетонами.
реакция Анри (или Генри, если французскую фамилию Henry читают как английское имя) – конденсация нитросоединений (метиленовая компонента) с альдегидами и иногда кетонами (карбонильная компонента). Сопряженное основание нитро-соединения (у этих анионов нет такого удобного названия как енолят для сопряженных оснований карбонильных соединений, их называют или нитронатами или солями аци-формы, и то, и другое не очень хорошо запоминается) – довольно слабый нуклеофил, что непосредственно следует из высокой стабильности этих анионов, поэтому реакции делают в основном с аальдегидами, а также самыми реакционноспособными кетонами (циклоалканонами, метилкетонами), так как реакции с более сложными кетонами обратимы и в равновесных смесях преобладают исходные. Конденсирующий агент – амины, карбонаты щелочным металлов, щелочи. Продукты – нитроспирты, если есть сопряжение с ароматическим кольцом – нитроолефины. Реакция с самым реакционноспособным альдегидом, формальдегидом, дает продукты полного замещения всех кислых протонов.

Нуклеофильности нитронатов не хватает для атаки на карбонильную группу сложных эфиров – аналога сложноэфирной конденсации в химии нитро-соединений нет.
Присоединение к электрофильным олефинам
После карбонильной группы следующим важным C-электрофилом является двойная связь, сопряженная с карбонилом или другим мезомерным акцептором. Мы хорошо знаем 1,4-присоединение разных нуклеофилов к таким связям (присоединение по Михаэлю). Анионы нитро-соединений не исключение. Это довольно полезная реакция. Кстати, в качестве активных олефинов могут выступать и нитро-олефины из реакции Анри.

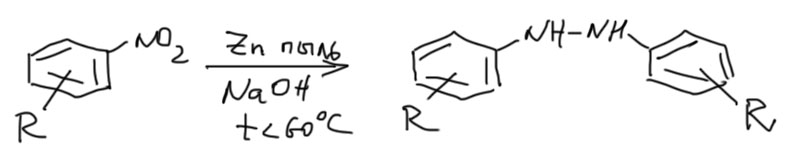
Сами исходные гидразины получаются двумя путями. Симметричные – просто восстановлением нитросоединений цинковой пылью в щелочной среде.
Несимметричные – гораздо более морочной процедурой. Для этого одна половина представлена соотвествующим анилином, вторая – нитрозобензолом. Нитрозосоединение пролучается в несколько стадий из нитросоединения, например, восстановлением до арилгидроксиламина, и окислением последнего, например, хлорным железом (еще годятся с десяток других окислителей, в частности надсерная кислота и трет-бутилгипохлорит, то есть так называемые переносчики положительного, в смысле электрофильного, кислорода). Полученные компоненты просто конденсируют в ледяной уксусной кислоте – это называется реакция Миллза, а азобензол восстанавливают цинком в щелочной среде.

Изменения реакционных центров
Синтез аминов
- Общие замечания
- Перегруппировки в реакциях Гофмана и Курциуса
- Синтез анилинов
- Введение вторичного алкила
- Введение первичного алкила
- Введение метила
- Перегруппировка Бекмана для синтеза аминов.
- Присоединение по Михаэлю в синтезе аминов
- Что не нужно делать
Второе обстоятельство связано с тем, что в аминах может быть до трех разных органических групп. Методы синтеза нужно подбирать в соответствии с природой этих групп. Можно воспользоваться вот таким несложным алгоритмом.
Строим амин RN(R”)R’
0. Амин циклический (азот в цикле) или нециклический, но с характерной особенностью – имеет два заместителя, отличающихся только CH2-группой (R и RCH2). Такой амин строится перегруппировкой Бекмана, а при наличии еще и третьего заместителя у азота переходим к шагу 4 и вводим его в последнюю очередь. Дальше пойдем по порядку.
1. Есть ли среди заместителей третичный алкил? Если нет, переходим к шагу 2. Если есть, допустим это R”, получаем сначала R”NH2 с помощью перегруппировок (реакции Гофмана или Курциуса) после чего переходим к шагу 3. Внимание: случай, когда в амине есть одновременно третичный алкил и его гомолог, например tBu и tBuCH2 уже описан в шаге 0. Внимание: в амине не должно быть больше одного третичного алкила. Если есть два или три, переходим к шагу 10. Если в оставшейся части есть ароматический заместитель, переходим к шагу 11.
2. Есть ли среди заместителей фенил или замещенный фенил. Если есть, допустим это опять R”, получаем сначала R”NH2 с помощью реакций, описанных на вкладке Синтез анилинов. Потом переходим к шагу 3. Внимание: а амине не должно быть больше одного ароматического заместителя – если есть два или три, переходим к шагу 11.
3. Внимательно осматриваем предложенный амин или остаток после шагов 1 и 2, а точнее каждый из оставшихся органических остатков. Что-то из них может оказаться сложным остатком, в котором после двух атомов углерода находится карбонил, карбоксил, амид, сложный эфир, нитрил, нитро-группа, или еще один амин. Это случай присоединения по Михаэлю. Таких остатков может быть до трех, и каждый навешиваем присоединением по Михаэлю. Внимание: выполнение нужно отложить до шага 6, а пока переходим к шагу 4.
4. Итак, в исходном амине не было ни третичного алкила, ни ароматического заместителя, или были, но мы их уже сделали. Продолжаем. Есть ли среди оставшихся заместителей вторичный алкил. Если есть, навешиваем с помощью восстановительного аминирования из соответствующего кетона. Если вторичных заместителей два или три, навешиваем в порядке уменьшения размера тем же способом. Если еще остались заместители, переходим к шагу 5.
5. Есть ли среди оставшихся заместителей первичные алкилы, но не метил. Если есть, навешиваем. Для этого используется много разных способов, смотрим их на вкладке Введение первичного алкила. Переходим к шагу 6.
6. Навешиваем сложные заместители присоединением по Михаэлю. Если необходимо, дополнительно их модифицируем. Переходим к шагу 7.
7. Остались, если остались, только метилы. Навешиваем метилы. Сравниваем результат с заданным амином. Если совпадает, радуемся. Если не совпадает, переходим к шагу 10.
8-9. В резерве. В текущей версии алгоритма не используются.
10. Выбрасываем белый флаг и начинаем горько плакать, так как задачу решить не удалось, и никто нам не поможет. Это провал.
11. Выбрасываем белый флаг и начинаем бурно возмущаться, потому что нас явно спрашивают о том, чего нет в программе. Это провокация!
В принципе, это вполне общий метод синтеза аминов, но он совершенно незаменим только в одном случае – когда с азотом связан третичный алкил. Еще этом метод иногда применяют для синтеза ароматических аминов, но только в том случае, когда не срабатывают более простые методы. Оба метода используют одну и ту же секстетную перегруппировку и одно и то же исходное – карбоновую кислоту.

Метод Гофмана отличается от Курциуса простотой (азид натрия есть не у всех, и желание получать азид и нагревать его с потенциальным риском досрочно отправиться на встречу с Курциусом, есть у еще меньшего количества разумных людей), и еще тем, что реакция заведомо идет в присутствии воды и в результате сразу получается искомый амин. А в Курциусе продуктом является не амин, а изоцианат, который нужно дополнительно гидролизовать. В остальном это одно и то же.
Реакцию используют для синтеза аминов через кислоты, например, через Гриньяр из третичного углерода (третичные алкильные Гриньяры вполне хорошо получаются обычным способом, хотя и труднее чем менее стерически затрудненные).


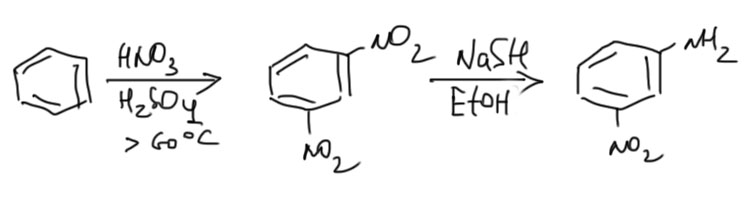
Есть еще одна важная реакция – частичное восстановление одной нитро-группы из нескольких. Для этого используют особый восстановитель – NaSH в спирте. При этом, реальное применение у этой реакции очень узкое – только такие молекулы, у которых не могут получиться разные продукты при восстановлении одной ниро-группы из нескольких. наиболее часто реакцию применяют для синтеза очень полезного в синтезе м-нитроанилина.
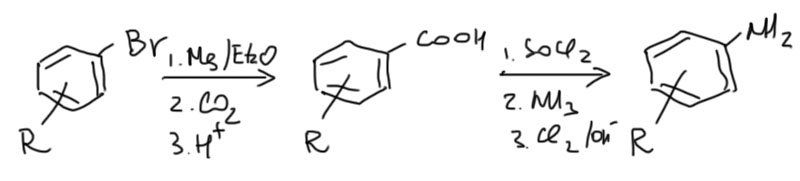
В редких случаях, когда по какой-то причине доступна бензойная кислота, можно получать анилины реакцией Гофмана. Например, так иногда бывает проще превратить ароматическое галогенпроизводное в анилин, так как нуклеофильное ароматическое замещение (освежите в памяти) – реакция непростая и часто осложняемая всякими странными процесами типа смещения входящей группы от места нахождения уходящей.
Кроме этого, неплохо не забывать про нуклеофильное ароматическое замещение.
Для восстановительного аминирования используют множество восстановителей, но нам можно ограничиться двумя. В простых случаях (когда вторичные алкилы суть что-то банальное типа изопропила, циклогексила и т.п.) это гетерогенное гидрирование водородом над никелем Ренея, в более сложных (это когда вторичный алкил может иметь дополнительные двойные связи или какие-то функциональные группы – спец. восстановитель цианоборгидрид натрия в слабокислой среде.
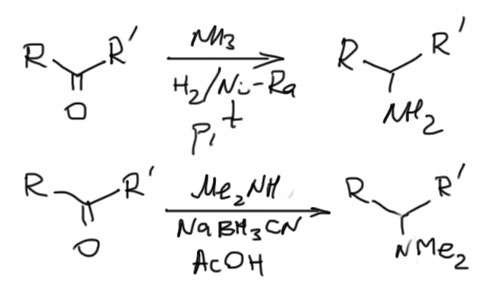
Если кетон енолизуемый, и вы еще не забыли, что такое енамин и можете его получить, то енамины отлично восстанавливаются обычным боргидридом натрия, но в этом случае заместитель будет последним, так как енамины образуются из вторичных аминов. Вот пример такого синтеза. Без этого подхода можно вполне обойтись, и все это сделать так, как описано выше без выделения енамина.

На первом месте востановление амидов карбоновых кислот или нитрилов алюмогидридом лития. Амиды легко получаются, при этом в амине могут уже быть другие заместители, нитрилы дают только амины с NH2-группой. Это очень надежный способ с огромным количеством реальных примеров применения.

Восстановление амидов используется и в подходе с использованием перегруппировки Бекмана на отдельной вкладке.
На втором месте восстановительное аминирование альдегидов, которое делается или так же, как и восстановительное аминирование кетонов, или, если в амине уже есть один заместитель, то получают основание Шиффа, и его восстанавливают боргидридом натрия.

Желательно этими методами и пользоваться. Но для аминов с незамещенной аминогруппой можно использовать еще и заместительные методы, в которых связь C-N образуется в результате SN2-замещения. В старинном методе Габриэля нуклеофилом является фталимид. Калийная соль фталимида – очень дешевый и доступный реактив, не требующий никаких специальных приемов работы. Но это очень скверный нуклеофил, поэтому реакции ведут, даже с самыми реакционноспособными бензилгалогенидами, в жестких условиях – при нагревании без растворителя. Получающийся N-алкилфталимид разлагают гидразином. Другой метод наоборот использует исключительно мощный нуклеофил – азид-ион, один из самых лучших нуклеофилов, известных человечеству. Реакции с азидом идут быстро даже с менее реакционноспособными алкилгалогенидами. Пока никто не видит, намекну, что он быстро реагирует даже с вторичными алкилгалогенидами. Получающийся азид разлагают трифенилфосфином (метод Штаудингера). Это – очень хороший и довольно универсальный, но дорогой и немного опасный (азиды очень токсичны) метод. Если хотите, используйте, но не забывайте проверять субстрат на пригодность для SN2.

Восстановительное аминирование формальдегида в присутствии муравьиной кислоты называется реакцией Эшвайлера-Кларка. Он никогда не дает четвертичных солей, как заместительное метилирование метилиодидом или диметилсульфатом, но все водороды будут заменены на метилы. Пока сделаем вид, что нам не приходит в голову, что может возникнуть задача заменить только один водород в NH2-группе на метил. 
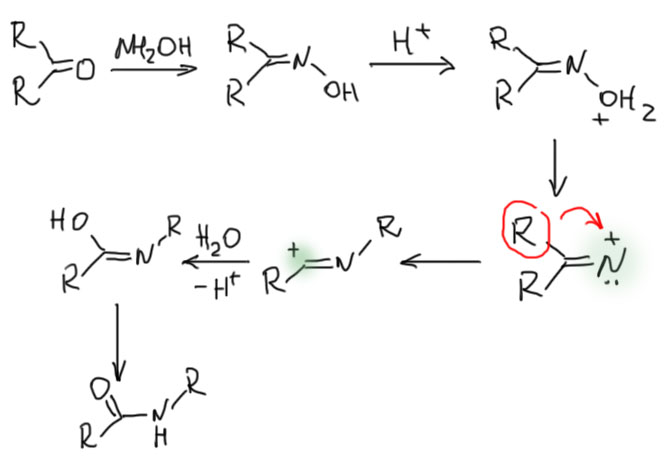
Как и в реакции Байера-Виллигера, и здесь лучше использовать симметричные кетоны, и по той же причине. Получающиеся амиды и сами по себе неплохие вещества, но их еще можно восстановить алюмогидридом лития до аминов. Амины при этом всегда получаются однотипные, и по этому признаку этот метод легко угадывается.
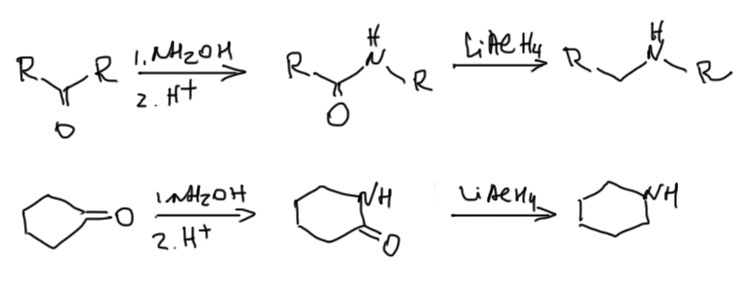
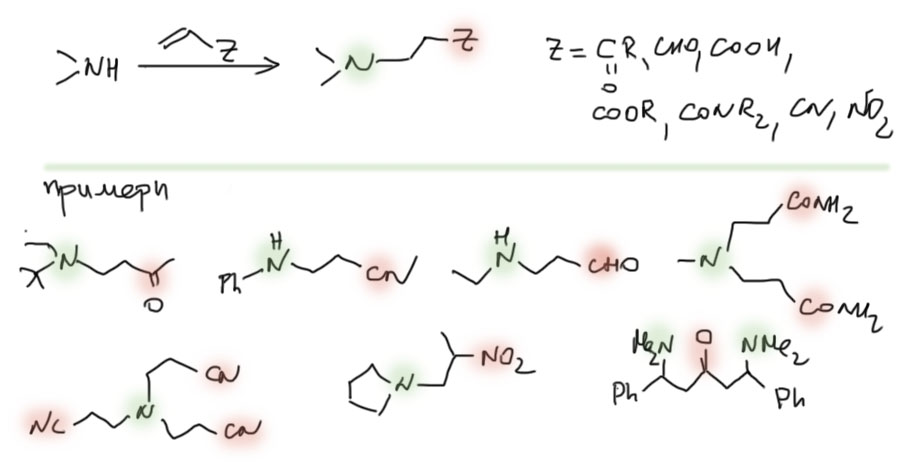
Но в полученных молекулах карбонилы, амиды, нитрилы, нитро-группы могут быть превращены в амины уже описанными методами. Получаются диамины или даже полиамины, у которых между аминами как правило три углерода, или два углерода, если была нитро-группа.
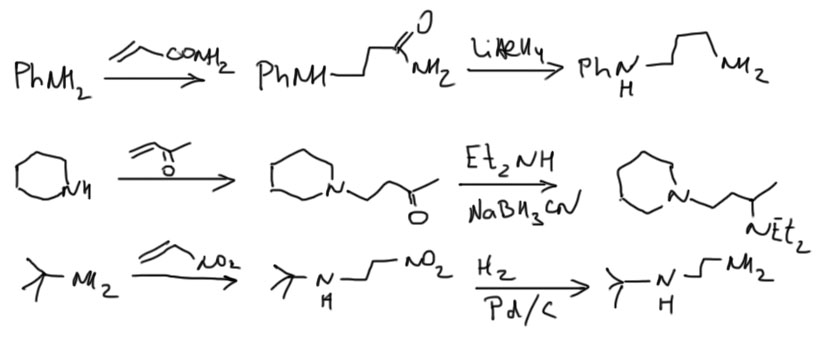
Те редкие случаи, когда заместительные реакции работают, перечислены на вкладках. Старайтесь не выходить за пределы рекомендованных методов.
Реакции солей диазония
- Выбираем...
- Термическое разложение солей диазония
- Восстановление солей диазония
- Реакции солей диазония с солями меди(1+) - реакция Зандмейера
Получение фенолов
Анион серной кислоты, бисульфат-ион, чрезвычайно слабый нуклеофил, как и положено аниону сильной кислоте. Поэтому в диазорастворе, полученном диазотированием с серной кислотой, нет другого нуклеофила кроме воды. В этом случае получаются фенолы. Диазораствор просто нагревают и выдерживают при кипении до полного разложения соли диазония. Чтобы в этом убедится, время от времени делают пробу на образование азокрасителя. Это – самый универсальный метод синтеза фенолов из доступных нам, хотя реакция довольно грязная и дает невысокие выходы просто потому, что соль диазония разлагается медленно, и по дороге начинает кусать образующийся фенол с образованием окрашенных смол.
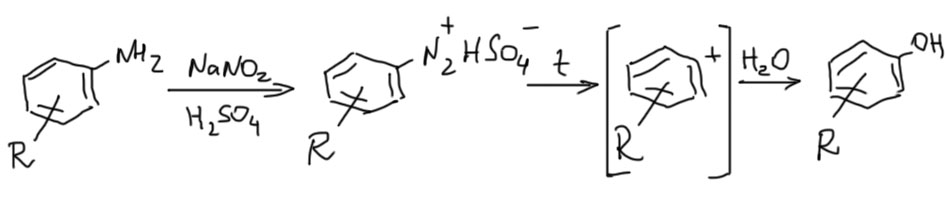
Получение фторпроизводных
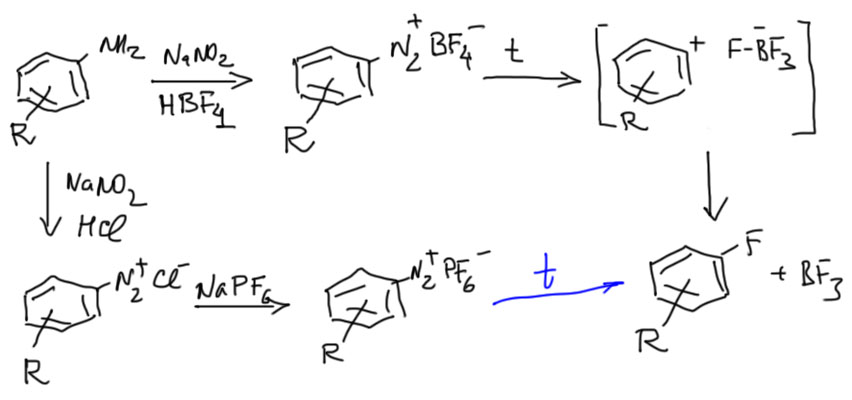
Фторид в качестве нуклеофила – штука крайне капризная и непростая. Можно было бы просто диазотировать в фтористоводородной кислоте, но она в водном растворе слабая, а с безводным фтористым водородом охотников работать немного. Поэтому пришлось использовать довольно неожиданный метод. Диазотируют в присутствии тетрафторборной кислоты – это легко доступный и дешевый реактив и получают тетрафторборат диазония. Альтернатива – диазотировать в соляной кислоте, и потом из водного раствора осаждать тетрафторборат солью тетрафторборной кислоты – немного дешевле, но и опаснее, потому что в такой соли диазония остаются ионы хлорида, что иногда приводит к взрывам при разложении. Вместо тетрафторборной кислоты или ее соли используют еще гексафторфосфорную кислоту, но это чисто косетическое, непринципиальное улучшение.
Соль выделяют и сушат и разлагают в твердом виде, просто нагревая смесь с чем-нибудь инертным, например, чистым отмытым и сухим песком (песок должен быть чистым! песок прямо из песочницы во дворе с хорошей долей вероятности сделает эксперимент последним). Тогда арильному катиону не остается ничего, кроме как выдрать фторид из тетрафторбората. Это очень трудно и красноречивее любых слов говорит о чудовищной реакционной способности катиона. Метод – реакция Бальца-Шимана – самый универсальный способ введения фтора в ароматическое кольцо. Видите фтор в ароматическом кольце – будьте уверены, что он там по вине Бальца и Шимана.
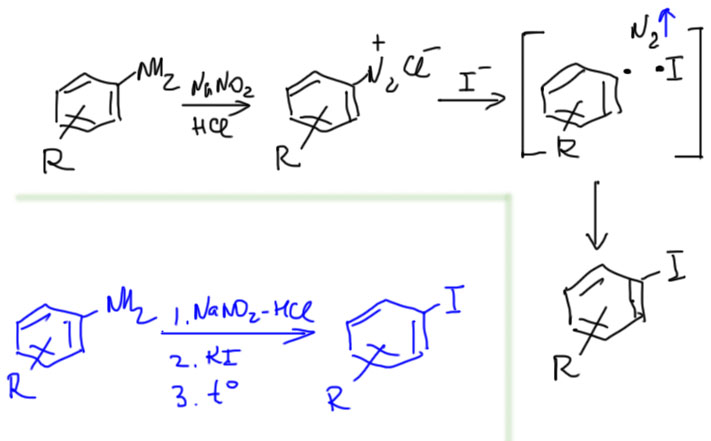
Другой важный способ превращать соли диазония во что-то полезное – реакция с восстановителями. Перенос электрона от восстановителя на соль диазония приводит к ее моментальному разложению с образованием того же азота и фенильного радикала. Радикал намного более стабильная (точнее, менее нестабильная) частица, чем катион, и такие реакции происходят намного легче термического разложения. Образующийся радикал быстро с чем-нибудь рекомбинирует, или выдирает атом водорода, откуда полегче. Таких реакций очень много, но мы возьмем самые важные.
Получение иодпроизводных
Уничтожение амино-группы
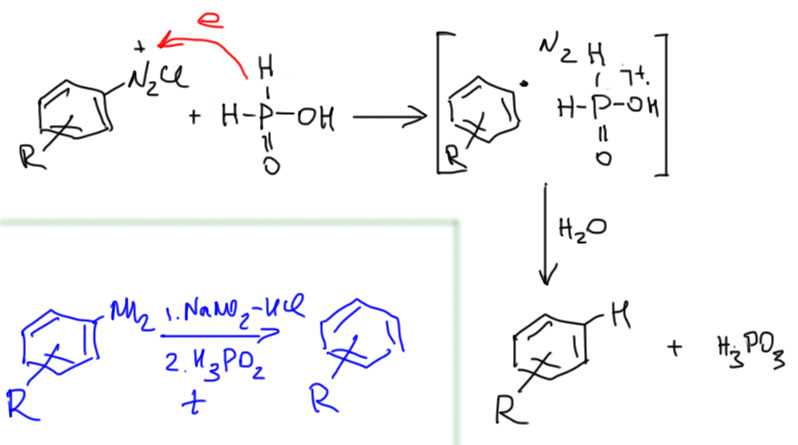
Это очень важная реакция в много стадийных синтезах, когда амино-группа используется как мощный ориентант, а затем удаляется. Такое превращение можно вызвать множеством реагентов, которые могут тыть источниками атома водорода – это и спирты, и боргидрид натрия, и т.п. – но самый надежный и универсальный – гипофосфористая кислота, которая по своей природе является фосфином, то есть содержит очень слабую связь P-H. Она же и восстановитель.
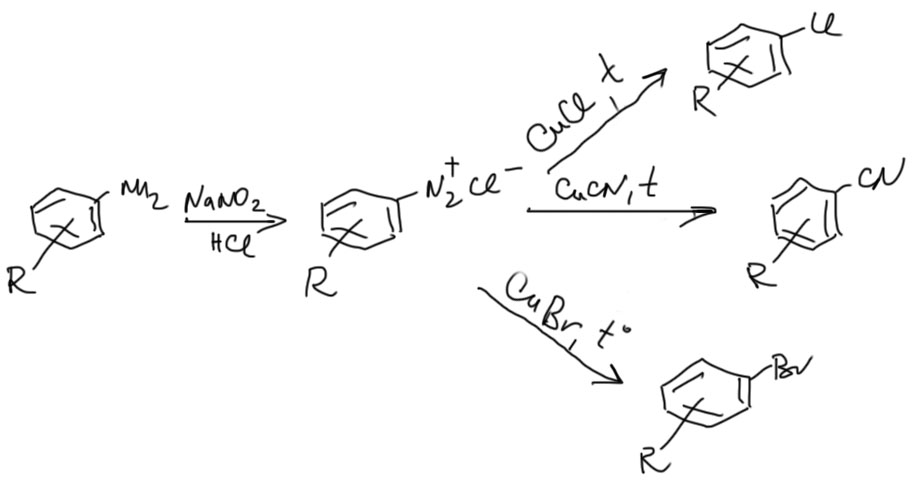
Но еще больше реакций солей диазония можно описать одним шаблоном – взаимодействие с производными одновалентной меди. При этом получаются производные с заменой диазогруппы на то, что было у меди. Механизмы этих реакций до сих пор толком неизвестны, но в любом случае это нечто для нас необычное, требующее рассуждений о реакциях в координационной сфере металла. Скорее всего, эти реакции, так же как и реакции с восстановителями, включают распад соли диазония до радикала, вполне вероятно за счет восстановления одновалентной медью, но дальше радикал не рекомбинирует, а получает один из лигандов с атома меди, который при этом переходит в Cu(2+). Даже писать это не будем.
Все эти реакции скопом называют реакцией Зандмейера. Так получают, среди прочего, хло-, бромпроизводные, и нитрилы.
Разные вспомогательные методы
Практически чистый путь элиминирования предложил еще в 19 веке как раз Гофман, ничего не зная ни про E2-механим, ни даже про основность. Но смысл его решения такой – нужно взять очень плохую уходящую группу, тогда и с основанием можно особенно не заморачиваться. В качестве уходящей группы используют триметиламин, а вся процедура выглядит как раз на 19 век: берем амин, обрабатываем его избытком иодистого метила – происходит три подряд SN2-замещения и образуется четвертичный аммоний с противоионом иодида. Обрабатываем это влажной окисью серебра, осаждается иодид серебра и получается гидроксид четвертичного аммония. Дальше просто греем и происходит E2-элиминирование. Если немного подумать, то можно придти к выводу, что гидроксид четвертичного аммония – это просто идеальные условия того, что мы сейчас называем межфазным переносом. И вспомнить. что в этих условиях гидроксид становится сильнейшим основанием, ничем не хуже трет-бутилата. Так что заодно мы выяснили, что Гофман со своим методом фактически предугадали межфазный катализ.
Так как уходящая группа очень плоха, но и работает как индуктивный акцептор, отщепление протона опережает уход плохой уходящей группы, и тогда важно, какой из имеющихся протонов более кислый – а это именно протоны на менее замещенном атоме углерода.

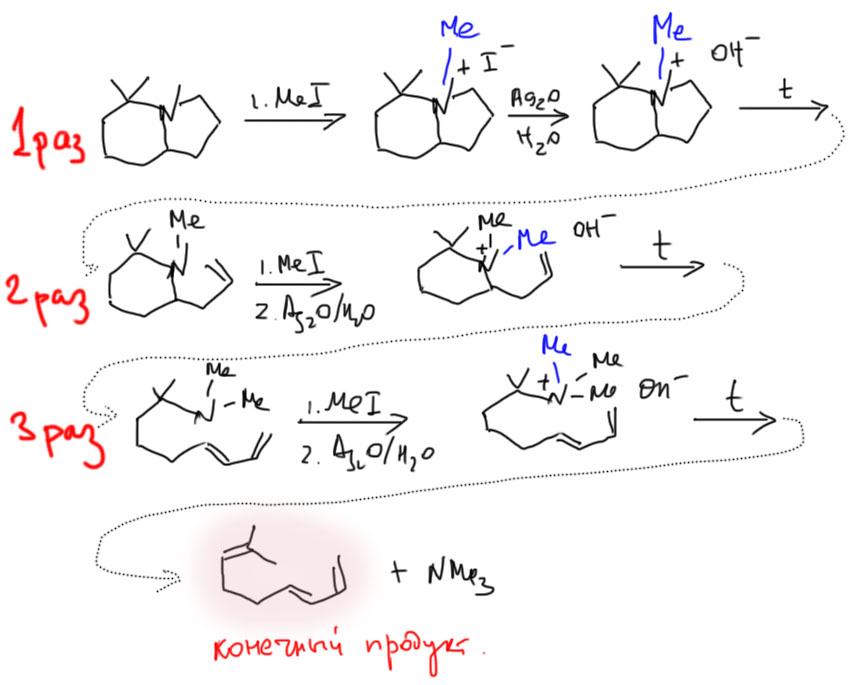
Этот метод очень активно использовали в доспектральные времена для установления структуры аминов. Проводили в несколько стадий полную деструкцию исходного амина, после чего исследовали полученное непредельное соединение. На каждой из стадий образуется наименее замещенный олефин из возможных. Так как основным приемом метода была обработка избытком иодистого метила, метод называли исчерпывающим метилированием. Вот пример применения метода – обратите внимание, в каком порядке образуются двойные связи из исходной структуры:
Алифатические нитро-соединения
- Из акролеина и нитрометана получите 1,5-динитропентан-2-ол
- Из бензальдегида и фенилнитрометана получите 1,3-динитро-1,2,3-трифенилпропан
Перегруппировка Бекмана и др.
2. Из дибензилкетона и ацетона получите бензил-изопропил-(2-фенилэтил)амин
Перегруппировки Гофмана, Курциуса и др.
2. Из циклогексанона, метилиодида и формальдегида получите 1-(N,N-диметиламино)-1-метилциклогексан
Присоединение по Михаэлю и др.
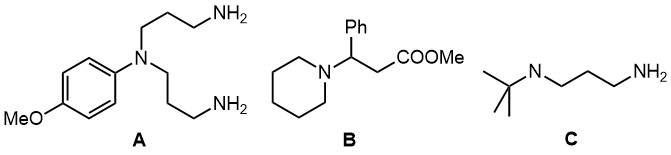
2. Из малоновой кислоты, бензальдегида, циклопентанона и диазометана получите соединение B (структура внизу)
3. Из акролеина и изобутилена получите диамин C.
Ароматические амины, восстановительное аминирование и др.
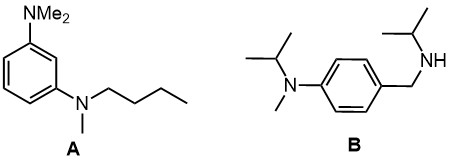
2. Из анилина, ацетона, формальдегида получите диамин B (структура внизу)
Диазотирование
2. Из 2,6-дидейтеробромбензола получите 3,5-дидейтеробромбензол
3. Из о-нитроанилина получите 1-фтор-3-хлор-4,6-дибромбензол
